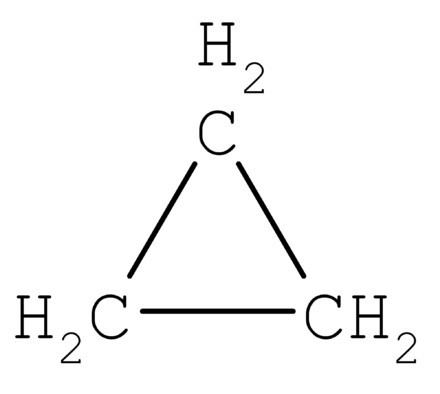
Производња ацетилена
Сигурно врло многи знају да је та реч -Ацетилен - повезан је са појмом "сирће". Али чињеница да је данас ацетилен - ово је једина супстанца која може запалити у одсуству ваздушног приступа, а која се широко користи у индустрији, а не сви знају. Ацетилен је опасан, наглашава се и чињеницом да, на пример, његово гашење у киселини ствара пламен са температуром до 3100 ° Ц.
По први пут је изведена производња ацетиленаЕдмунд Давеи у далеку 1836. Деви је деловао на калијум карбиду са обичним воденим раствором, дошло је до реакције која се може записати као: К2Ц2 + 2Х2О = Ц2Х2 + 2КОХ. Као резултат, добијен је гас, чија формула је Ц2Х2 и на коју је научник назвао бикарбонатни водоник.
Откривањем доктрине радикала Јустуса Лиебигаиз група атома (радикала) и названа ацетил, иако је сматрао једињење формуле Ц2Х3. Супстанца која је примила Деви почела је да разматрају хемичари као дериват ацетила. Затим, када је куповину ацетилена француски Марцелен Бертхелот извршио на неколико начина, супстанца је добила своје име, које се данас користи у хемији. Бертхелот сматра резултујуће једињење као молекул ацетила из којег је узет атом водоника. Технолошки је производња ацетилена Бертхелот био следећи процес. Прошао је пар загрејаних алкохола - метил и етил - кроз цев такое загрејан на високој температури.
Неколико касније, 1862. године, био је ацетиленсинтетизовано електрохемијском реакцијом, током којег је водоник пролазио између електрода направљених од угљеника. Ове технологије у то време биле су веома скупе и неефикасне, те се стога могле сматрати само као теоретско решење проблема. Само на самом крају века пре последњег изумио је метод који је омогућио успостављање економичније аквизиције ацетилена. Ова метода се заснива на паљењу смеше која се састоји од гипса и угља. То нам је омогућило да подесите употребу прикључка као гас за улично осветљење. Чињеница је да је гас, који је садржао око 92,3% угљеника, на високој температури, оставио велику количину ове супстанце у чврстом облику. Дају довољно светлости. У овом случају температура сагоревања одређује не само осветљење горења, већ и њену боју. Што је температура већа - раније је боја сјаја угљеничних честица. Појављени грејачи, напуњени ацетиленом, могу дати светлост око петнаест пута више од тада распрострањених плинских светала. Чак и када су их заменили електричним осветљењем, употреба ацетилена за осветљење настављена је у бочним лантернама и омнибусима.
Како је индустрија развијала свевелике количине таквих једињења као што је ацетилен. Добијање у индустријским количинама почело је тек у прошлом веку. Као резултат овог "продора", веза се такође користи за техничке потребе. За потребе зграде, ацетилен је произведен каљењем карбида водом. Овај производ је познат по веома непријатном мирису због присуства амонијака и водоник сулфида у њему. У ствари, хемијски чиста супстанца има слабо изражени етеричан мирис. Лакша је од ваздуха, молекуларна маса ацетилена је 26.038. Гас нема боју, лако је растворљив у многим течним растворима, а растворљивост се одређује температуром самог решења.
Модерне технологије обезбеђујуацетилен из метана помоћу електрокрекинга, процес у којем се метан гас прво преноси између електрода на температури нижу од 1600 ° Ц. Затим, како би се спречило распадање ацетилена, гас се подвргава брзом хлађењу. Такав поступак је ефикасан у оном делу топлоте која се генерише сагоревањем супстанце може се усмјерити на загријавање сљедећег реакционог циклуса, осигуравајући континуирану природу његовог тока.
Ацетилен се широко користи у области заваривања и сечења метала, да се добије веома светао белу светлост, за производњу експлозивних материја.
</ п>